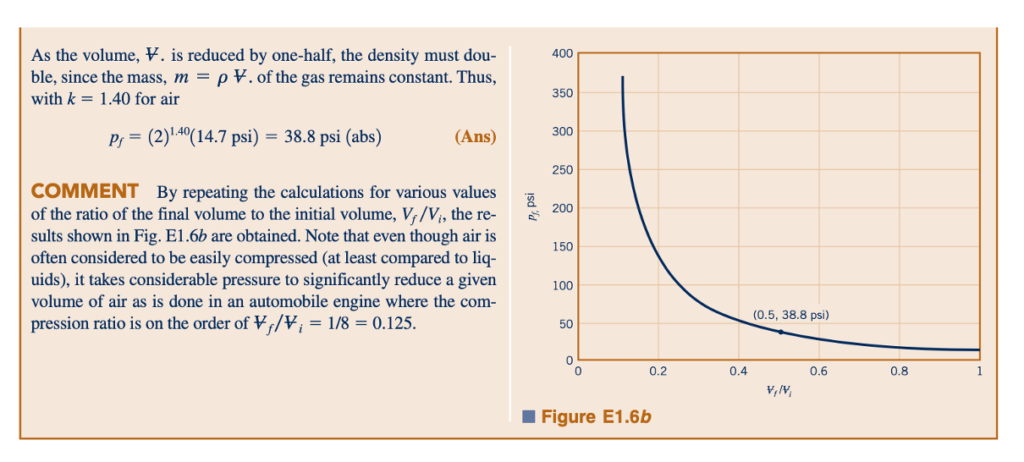
Kompresi dan Ekspansi Gas
Ketika gas dipadatkan (atau diperluas), hubungan antara tekanan dan kerapatan tergantung pada sifat dari proses tersebut. Jika kompresi atau ekspansi terjadi di bawah kondisi suhu konstan (proses isotermal), maka dari Persamaan 1.8

Jika kompresi atau ekspansi berlangsung tanpa gesekan dan tidak ada pertukaran panas dengan lingkungan sekitarnya (proses isentropik), maka
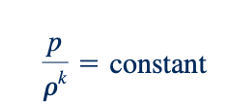
di mana k adalah rasio panas spesifik pada tekanan konstan, cp terhadap panas spesifik pada volume konstan, cv (yaitu, k= cp/cv). Dua panas spesifik ini berhubungan dengan konstanta gas, R, melalui persamaan R= cp−cv . Seperti halnya dalam hukum gas ideal, tekanan dalam kedua Persamaan 1.14 dan 1.15 harus diekspresikan sebagai tekanan absolut. Nilai-nilai k untuk beberapa gas umum diberikan dalam Tabel 1.7 dan 1.8, dan untuk udara pada berbagai rentang suhu, dalam Lampiran B (Tabel B.3 dan B.42). Variasi tekanan-kepadatan untuk kondisi isotermal dan isentropik diilustrasikan dalam gambar di pinggir.
Dengan persamaan eksplisit yang menghubungkan tekanan dan kepadatan, modulus bulk untuk gas dapat ditentukan dengan mendapatkan turunan dp/dp dari Persamaan 1.14 atau 1.15 dan mensubstitusikan hasilnya ke dalam Persamaan 1.13. Ini mengikuti bahwa untuk suatu proses isotermal
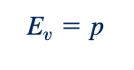
dan untuk suatu proses isentropik,
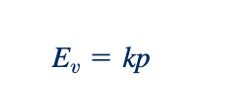
Perhatikan bahwa dalam kedua kasus tersebut, modulus bulk bervariasi secara langsung dengan tekanan. Untuk udara dalam kondisi atmosfer standar dengan p =14.7 psi (abs) dan k=1.40, modulus bulk isentropik adalah 20.6 psi. Perbandingan angka ini dengan angka untuk air dalam kondisi yang sama (Ev =312,000 psi) menunjukkan bahwa udara kira-kira 15,000 kali lebih dapat dipadatkan dibandingkan dengan air. Oleh karena itu, jelas bahwa dalam menangani gas, perhatian lebih besar perlu diberikan terhadap efek kompresibilitas pada perilaku fluida. Namun, seperti yang akan dibahas lebih lanjut dalam bagian-bagian selanjutnya, gas sering kali dapat diperlakukan sebagai fluida tidak dapat dipadatkan jika perubahan tekanan kecil.